IVT RNA医薬品開発
ベクタービルダーは、ワクチン、遺伝子置換、 キメラ抗原受容体(CAR)、遺伝子編集を含むRNA治療薬開発のための包括的なプラットフォームを提供しています。当社の専門家チームは、治療デザインおよびプロセス開発における重要な検討事項についての豊富な知識を基づいてRNA医薬品の有効性、安全性、製造可能性を高めることができます。またRNA医薬品の大規模製造は、弊社の CDMOサービスをご覧ください。
Talk to Our Experts




IVTベクター
デザイン & クローニング
デザイン & クローニング
IVT RNA製造
LNPカプセル化
品質管理 (QC)
機能検証
IVTベクターデザイン & クローニング
- 商業利用のためのIP制約のないロイヤリティフリーのIVTバックボーン
- 独自の配列最適化による最適な発現
- 120nt(およびそれ以上)のポリAテールの安定したクローニングと転写
- UTR最適化
- コーディング配列最適化
- ポリA安定性
- ポリA長とGOI発現
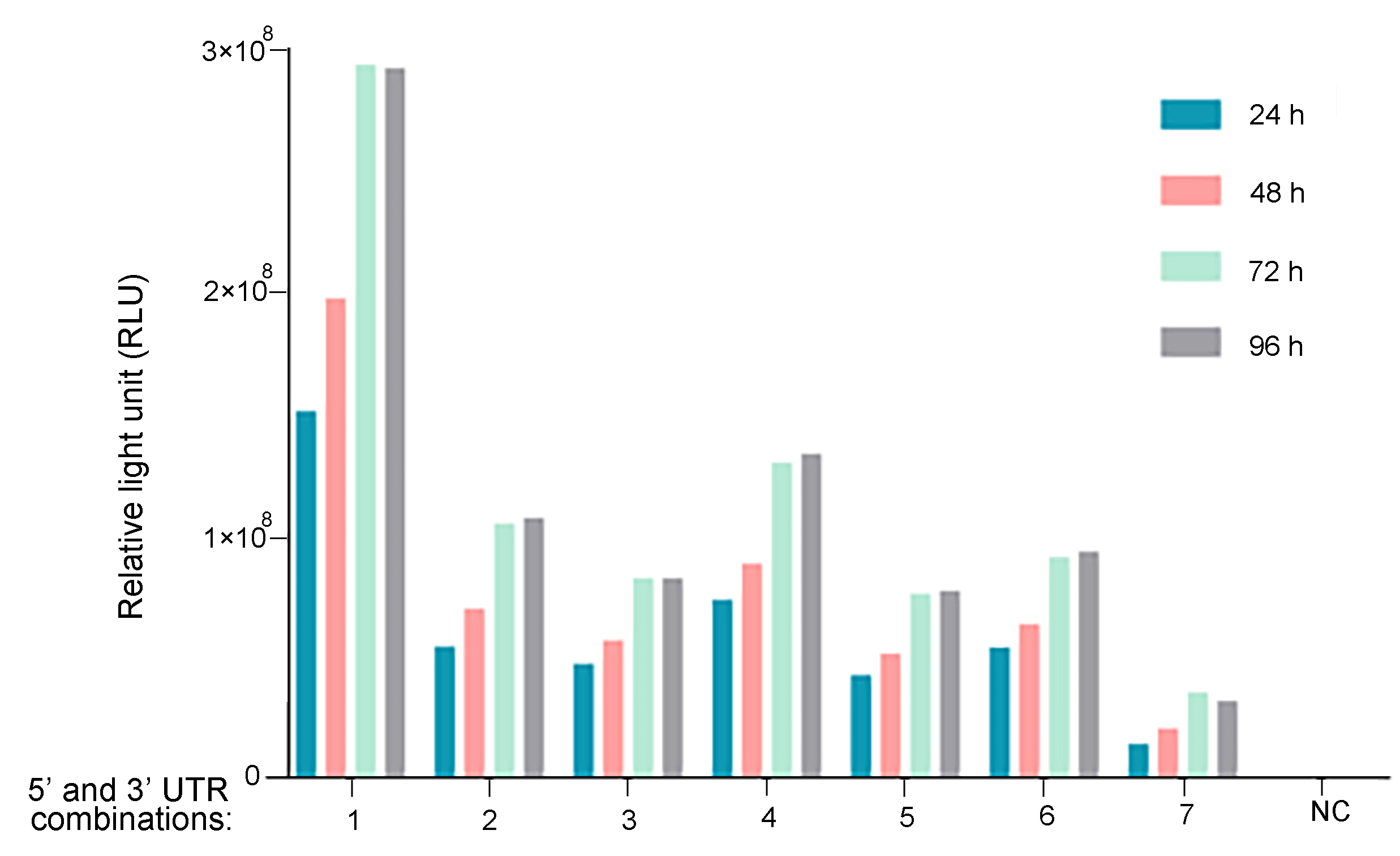
図 1. UTR最適化によるmRNA発現の改善。様々な5'UTRと3'UTRの組み合わせによる、in vitroでガウシアルシフェラーゼ発現への影響を調査した。HEK293T細胞を12ウェルプレートに2.3x10^5細胞/ウェルの密度で播種し、1ug mRNAを添加した。トランスフェクション後6,24、48、72、96時間後に、培養液中のガウシアルシフェラーゼ活性を測定した。
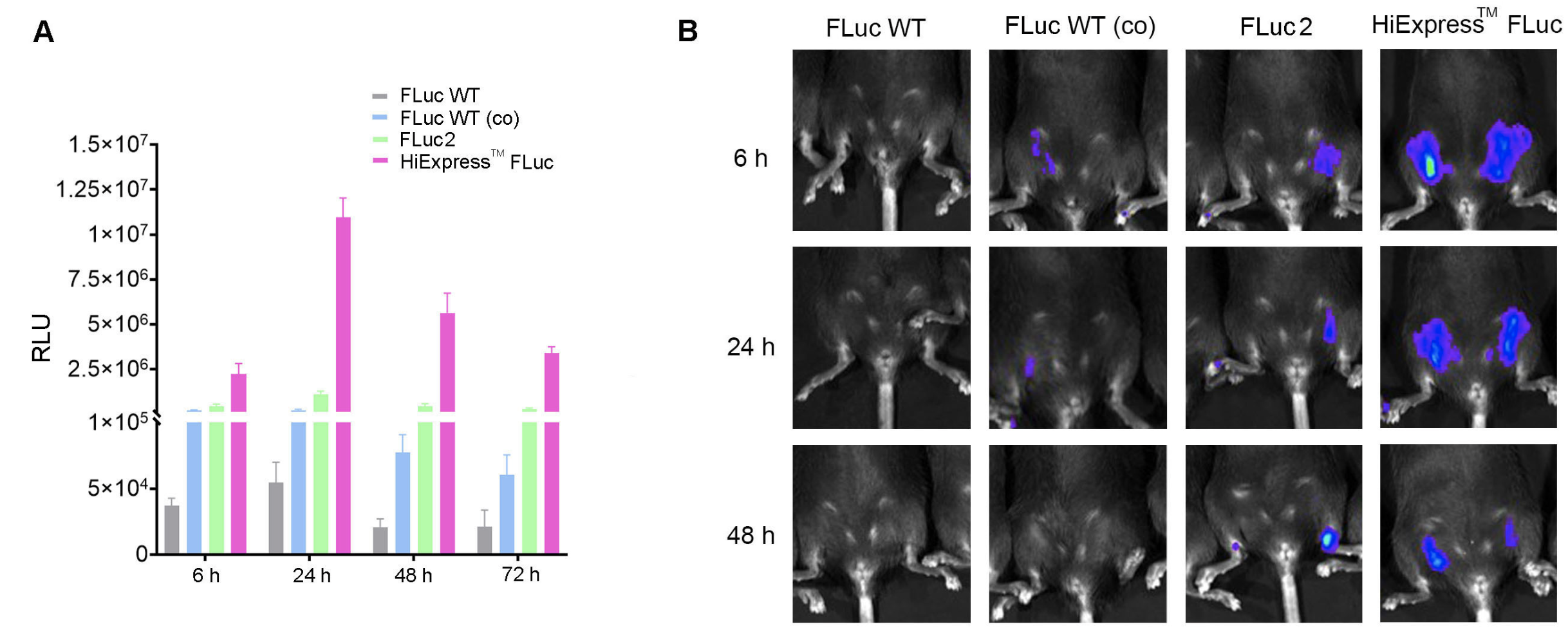
図 2. コドン最適化による、in vitroおよびin vivoでのmRNA発現量の増加。(A)HEK293T細胞におけるHiExpress™ ホタルルシフェラーゼmRNAおよび他のルシフェラーゼmRNAの発現。12ウェルプレート上で培養中の細胞を、1ウェルあたり0.5ugのmRNAでトランスフェクションし、ルシフェラーゼ活性を6時間、24時間、48時間、72時間後に測定した。(B)成体C57BL/6マウスに30ugのLNP-mRNAを筋肉内注射し、6時間、24時間、48時間後にルシフェラーゼ活性を測定した。FLuc WTは野生型ホタルルシフェラーゼ、FLuc WT(co)はコドン最適化された野生型ホタルルシフェラーゼ、FLuc2はLuc2ホタルルシフェラーゼを示す。
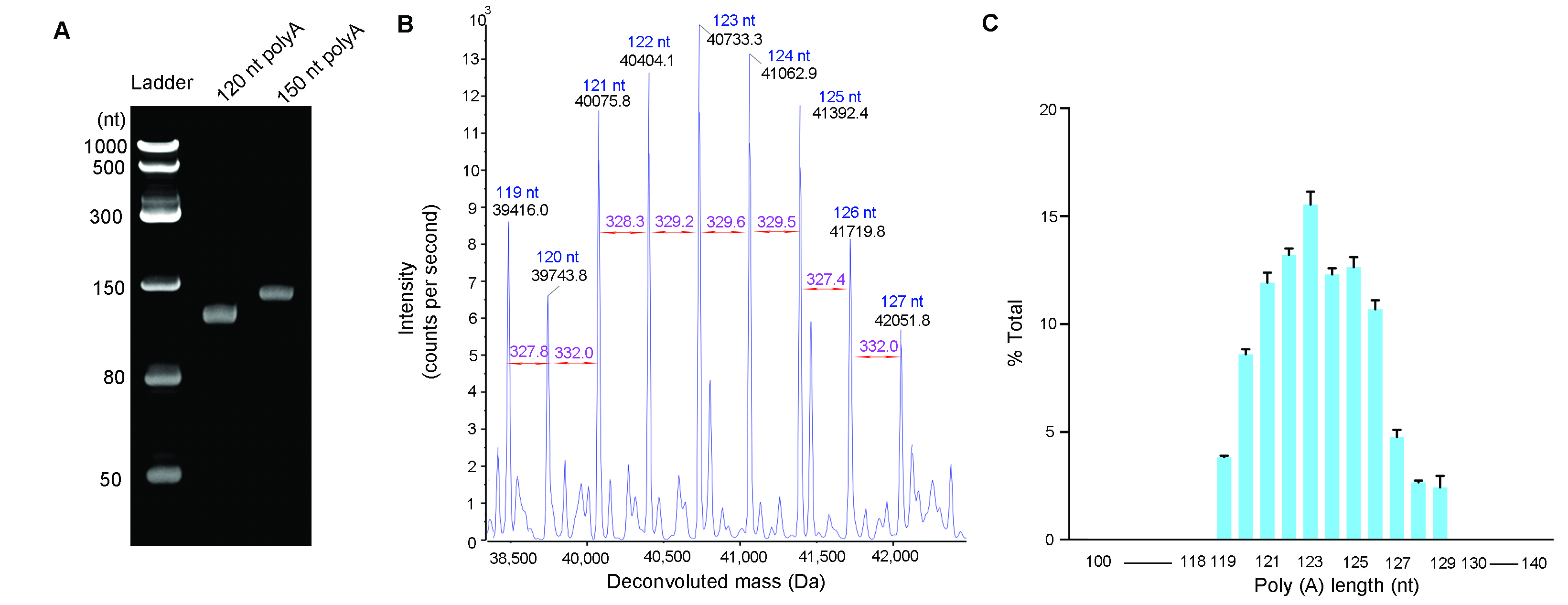
図 3. ポリAテールのサイズ解析。ポリAテールはリボヌクレアーゼT1を用いてIVT mRNAから切断し、オリゴdTアフィニティークロマトグラフィーで単離した。(A) 単離されたポリAテールのUrea-PAGEゲル電気泳動解析。(B)単離ポリA末端のLC-MS分析。デコンボリューションされたスペクトルから120ntのポリAテールが生成された。(C)120ntポリAテールのサイズ分布。エラーバーはトリプリケートからの標準偏差を表す。長さび加重平均は123 ntだった。
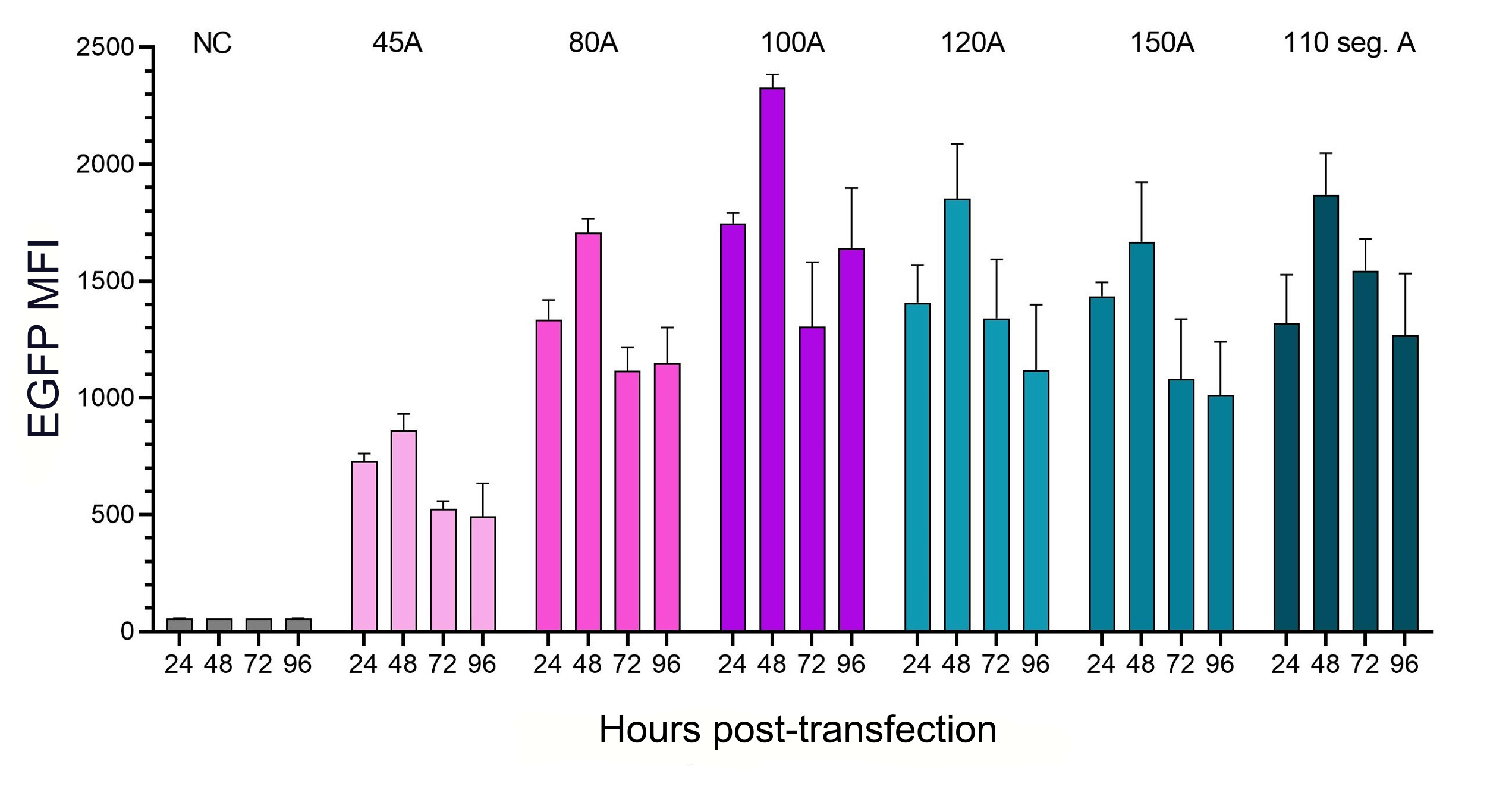
図 4. ポリAの長さと構造の翻訳効率に対する影響。同じCap1とUTRを持つが様々なポリAテール長を持つIVT EGFP mRNAをHEK293T細胞にトランスフェクションした。
IVT RNA製造
- ベクターのクローニングからLNPカプセル化まで最速5週間でお届け
- マイクログラムからグラム量まで、最大10,000 ntのmRNAとsaRNA、および5,000 ntのcircRNA製造
- 共転写法または酵素法による高いキャッピング効率(99%まで)
- 様々な修飾ヌクレオチドオプション(m1Ψ、m5C、5moUなど)
- 独自の精製技術によって不純物を効率的に除去
- 包括的なQCパネル
- IVT鋳型DNAの無細胞生産システムを提供することで、大規模IVT RNA製造の生産時間を大幅に短縮
- mRNA安定性
- キャッピング効率
- 修飾ヌクレオチド
- dsRNA除去
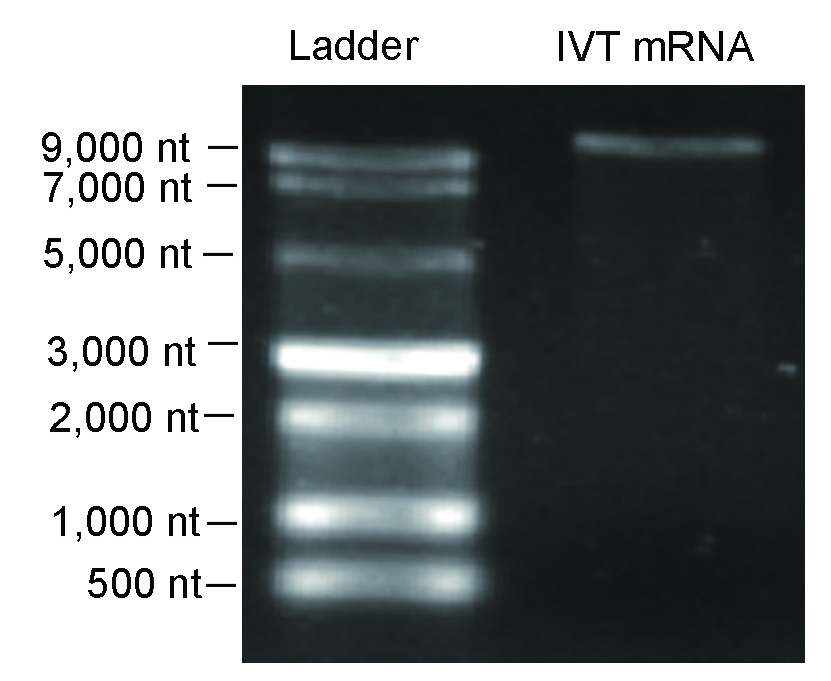
図 5. 安定性の高い10,000 ntを超えるIVT RNAの変性アガロース電気泳動像
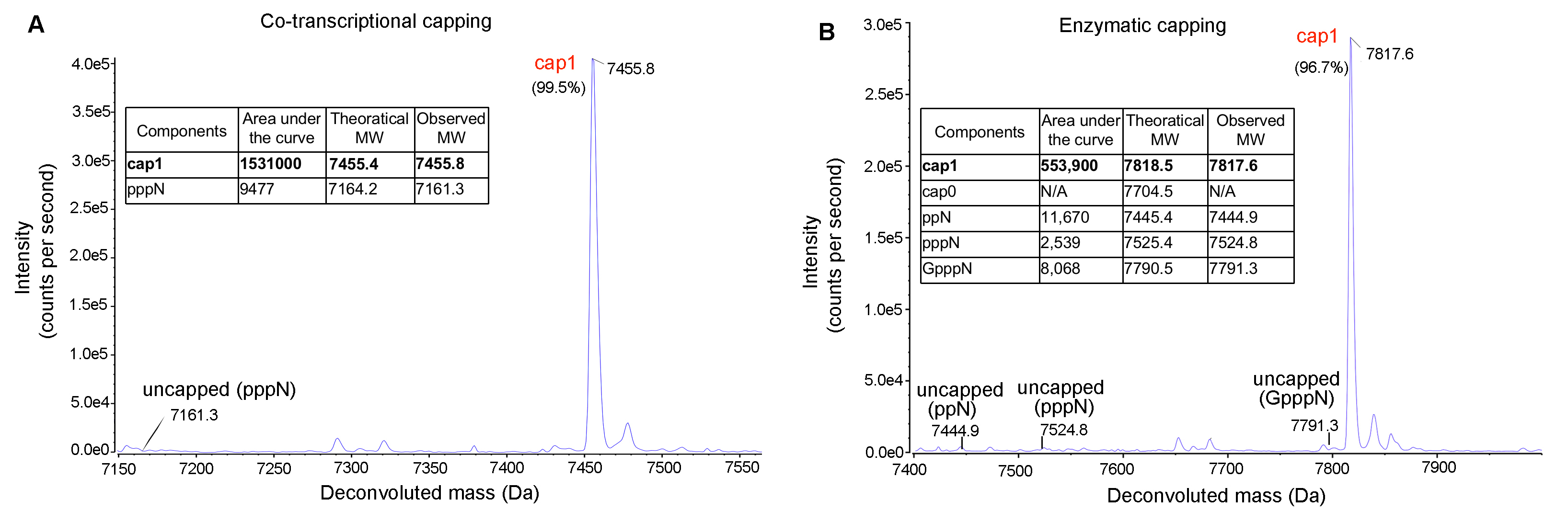
図 6. LC-MSで解析したIVT mRNAのキャッピング効率のLC-MS解析結果。(A)共転写法または(B)酵素法のいずれを用いても、高効率のキャッピング(>99%)が達成された。
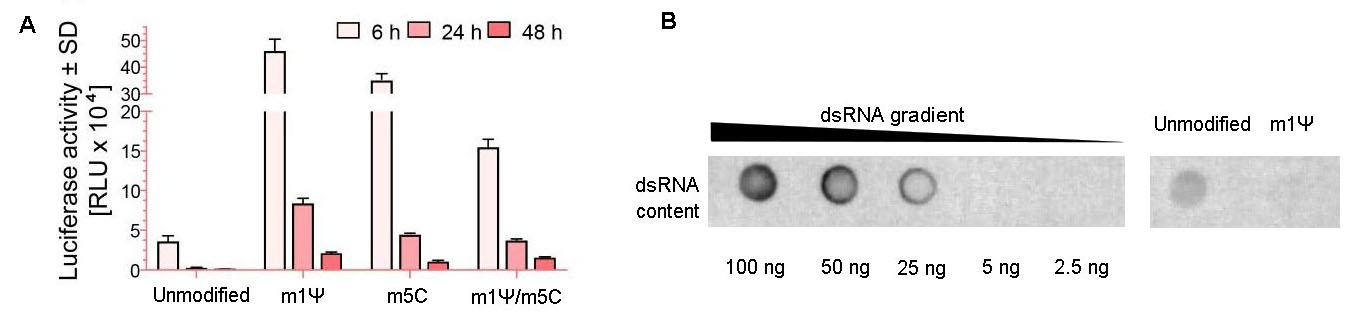
図 7. 修飾ヌクレオチドはmRNAの発現量を増加させ、dsRNAの不純物を低減する。(A)HEK293T細胞におけるホタルルシフェラーゼの発現。修飾ヌクレオチド(N1-メチルシュードウリジン(m1Ψ)および5-メチルシトシン(m5C))の有り/無しのmRNAを合成した。細胞は12ウェルプレートで増殖させ、1ウェルあたり1ugのmRNAをトランスフェクションした。トランスフェクション後6時間、24時間、48時間におけるHEK293T細胞のルシフェラーゼ活性を測定した。エラーバーは標準偏差を示す。(B)ヌクレオチド修飾(m1Ψ)有り/無しのEGFP IVT mRNAを磁気ビーズ精製した後にdsRNA 不純物についてドットブロットアッセイ(750 ng/ドット)で分析した。
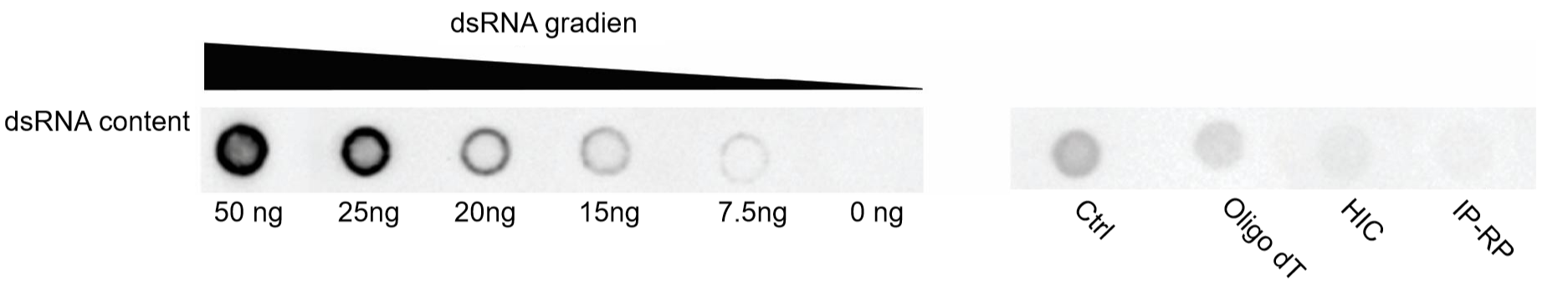
図 8. 精製プロセスの違いによる dsRNA 除去効率。異なる方法で精製したhSpCas9 IVT mRNAをドットブロットアッセイ(1ドットあたり1500 ng)で評価し、dsRNAの不純物を推定した。略号 HIC, 疎水性相互作用クロマトグラフィー; IP-RP, イオンペア逆相液体クロマトグラフィー。
LNPカプセル化
詳細は LNPカプセル化 サービスのページをご覧ください。
品質管理(QC)
ベクタービルダーはIVT RNA用のあらゆるQCアッセイを提供しています。デフォルトのQC項目(√印)に加えて、オプションQC項目は個々のプロジェクトのニーズに応じて実行されます。
| 検査対象 | QCアッセイ | リサーチグレード | GMP-like | |
|---|---|---|---|---|
| 同質性・同等性 | mRNA配列 | サンガーシークエンス | √ | √ |
| mRNA長 | 変性ゲル電気泳動 | √ | √ | |
| キャピラリーゲル電気泳動(CGE) | オプション | √ | ||
| 一般/物理的性質 | mRNA濃度 | UV分光光度法 | √ | √ |
| RiboGreenアッセイ | オプション | √ | ||
| 外見 | 目視による検査 | オプション | √ | |
| 機能 | 遺伝子発現 | In vitro翻訳とウェスタンブロット | オプション | オプション |
| 細胞へのトランスフェクション | オプション | オプション | ||
| 安全性 | 無菌性 | バイオバーデン試験 | オプション | √ |
| マイコプラズマ | 培養法 | オプション | √ | |
| qPCR | オプション | オプション | ||
| エンドトキシン | キネティッククロモジェニック(KCA) | オプション | √ | |
| 純度 | mRNA安定性 | 変性アガロースゲル電気泳動 | √ | √ |
| キャピラリーゲル電気泳動 (CGE) | オプション | √ | ||
| A260/280 | UV 分光光度法 | √ | √ | |
| キャッピング効率 | LC-MS | オプション | √ | |
| ポリA解析 | LC-MS | オプション | √ | |
| 残存dsRNA | ドットブロット法 | オプション | √ | |
| 残存プラスミドDNA | qPCR | オプション | √ | |
| 残存タンパク質 | NanoOrange アッセイ | オプション | √ | |
| 残存試薬 | ガスクロマトグラフィー | オプション | オプション | |
| 環状化効率 (circRNAの場合) | 変性アガロースゲル電気泳動 | √ | オプション | |
| キャピラリーゲル電気泳動(CGE) | オプション | √ | ||
機能検証
ベクタービルダーの科学者と技術チームは、治療目的に最適なIVT RNAを設計するための機能研究をサポートしています。
- 様々なベクターコンポーネント(UTR、コード配列、ポリA、コザック配列など)の最適化の効果をin vitroおよびin vivo評価。
- 抗原提示、抗体発現、CAR発現、CRISPRなど様々な用途のIVT RNAの検証
- げっ歯類や非ヒト霊長類(NHP)を含む動物モデルを用いたLNP遺伝子導入の有効性と安全性評価