プラスミドDNA製造

VectorBuilderは、遺伝子治療開発パイプライン全工程を通じて、プラスミドデザイン、クローニング、製造のあらゆるニーズに対応します。VectorBuilderの革命的な ベクターデザインプラットフォーム の利用と、当社の豊富な経験に基づいて、研究と臨床ニーズに合致した最適なベクターデザインと製品をご提供します。 プラスミドDNA製造では、創薬研究、前臨床研究、臨床試験、商品化など、様々なニーズに対応できるようダウンストリームサービスをそろえ、複数のプラスミドDNAのグレードをご提供しています。
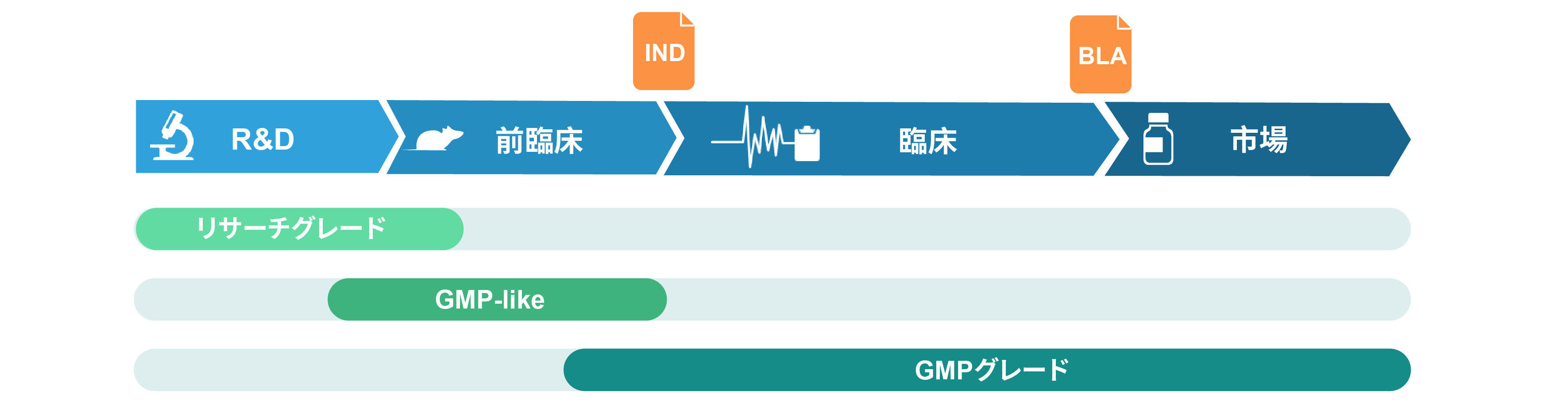
提供しているプラスミドDNAのグレード
-
リサーチグレード プラスミド
リサーチグレードのプラスミドDNAは、基礎研究及び創薬研究を目的としています。全てのダウンストリームの研究ニーズに適した高品質を保証するために、厳しいQCチェックを備えた標準的な実験室条件下で製造します。.
リサーチグレードプラスミドサービスを読む -
GMP-like プラスミド
GMP-likeプラスミドDNAは、薬物の安全性と代謝研究のための動物実験などの前臨床研究を目的使用を目的としています。これはGMPガイドラインのうち主要な項目を満たす条件で製造され、GMPと同等の製造プロセスで製造され、同等の品質を満たすプラスミドDNAとなっています。プラスミドDNAの製造は、ドキュメント管理と、トレーサビリティーを備えた、隔離製造スイートで行われます。したがって GMP-likeグレードでは最終的なGMP製品をスモールスケールで模倣しているとみなせます。GMP-likeグレードの特長は、GMPに比べてコストがはるかに低く、タイムラインも短縮されます。必要に応じて、GMP-likeプラスミドは、抗生物質フリー、RNaseフリーのファーメンテーションおよび精製条件下で生成できます。品質検査証明書(certificate of analysis :COA) が、製品のリリース時に発行されます。ご依頼に応じてTSE/BSE証明書も発行します。
-
GMP プラスミド
GMPグレードのプラスミドDNAは、GMPガイドラインに厳密に準拠した認定GMPスイートで製造されます。包括的な品質保証システムが製造プロセス全体に実施されます。プラスミドDNAが目的の品質および安全基準を満たしているか、または超えていることを確認するために、様々なインプロセス(in-process)およびリリースQCアッセイが実施されます。製品リリース時には、品質検査証明書(Certificate of analysis: COA)と、製造プロセスを漏らすことなくドキュメント化したバッチリリース報告書が発行されます。
プラスミドDNAグレードの比較
| リサーチグレード | GMP-like | GMPグレード | |
|---|---|---|---|
| アプリケーション | 基礎研究, 治療薬開発, および 前臨床研究 | 薬物の安全性や代謝に関する動物を使った前臨床試験、GLP試験 | 前臨床試験, 臨床試験, および商用 |
| 製造スケール | 10ugから数百mg | バッチごとに10mgから1g | バッチごとに10 mg から 5 g まで |
| 作業日数 | 1-8 日 | 1-3 カ月 | 数カ月~半年 |
| 品質管理システム | ISO9001 | GMP製造の主要な特長を取り入れた ISO9001 | GMP製造のためのICH品質ガイドライン |
| 製造場所 | 標準的な実験室での並行生産 | 隔離された製造スイートで製造 | 認証されたGMPスイートで製造 |
| 文書管理とトレーサビリティ | なし | あり | 全ての工程においてあり |
| QCおよび出荷時検査 | 濃度測定、 OD260/280、 制限酵素処理 |
個々のプロジェクトのニーズに合わせて実施 | 全てのQCアッセイを実施、および 個々のプロジェクトのニーズに合わせた解析 |
| 無菌充填 | N/A | 要望があれば可能 | あり |
| サンプルの保存 | 要望があれば可能 | 要望があれば可能 | あり |
| 交付書類 | COA(要望があった場合のみ) | 1. COA 2. 製造サマリー 3. TSE/BSE 文書(要望があった場合のみ) |
1. COA 2. TSE/BSE 文書 3. CTD文書 (CommonTechnicalDocument) 4. BMR 等、 その他リクエストに応じて対応 |
GMPウイルス製造のワークフロー
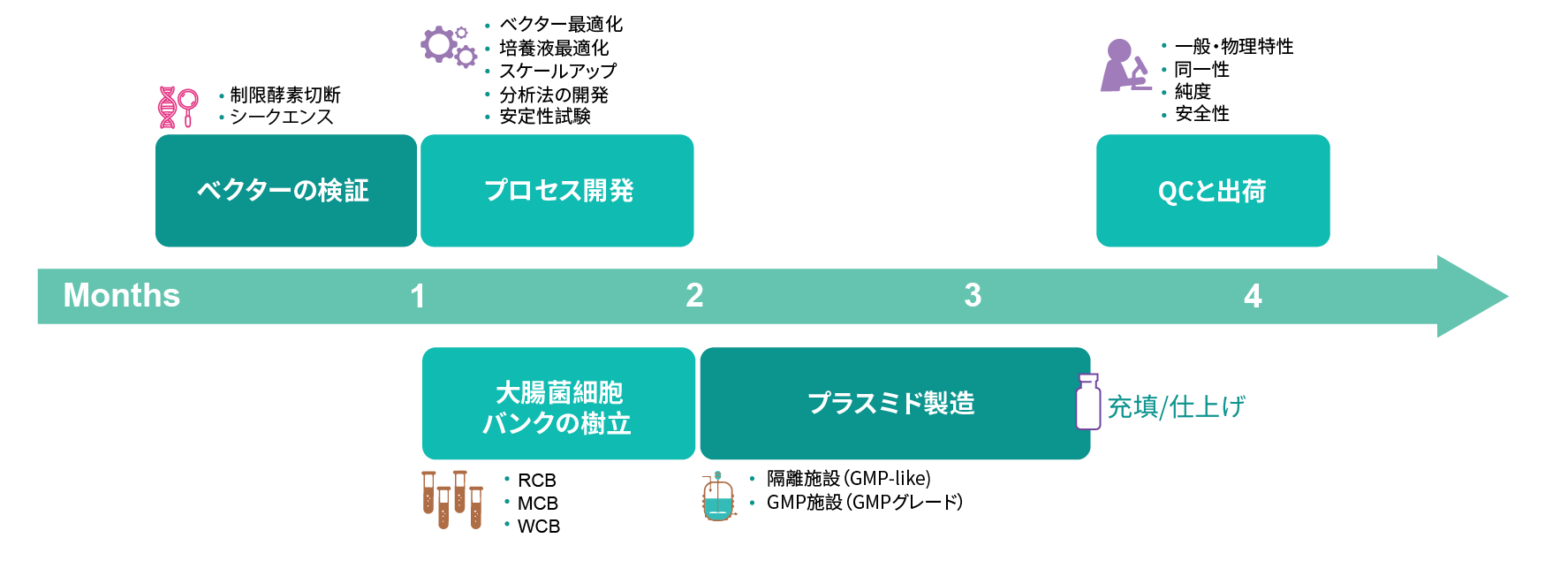
VectorBuilderは、品質の良い製品を納期通りにお届けすることに努めています。 ここにプラスミドDNAの典型的なGMP製造ワークフローを示します:
テクノロジープラットフォーム
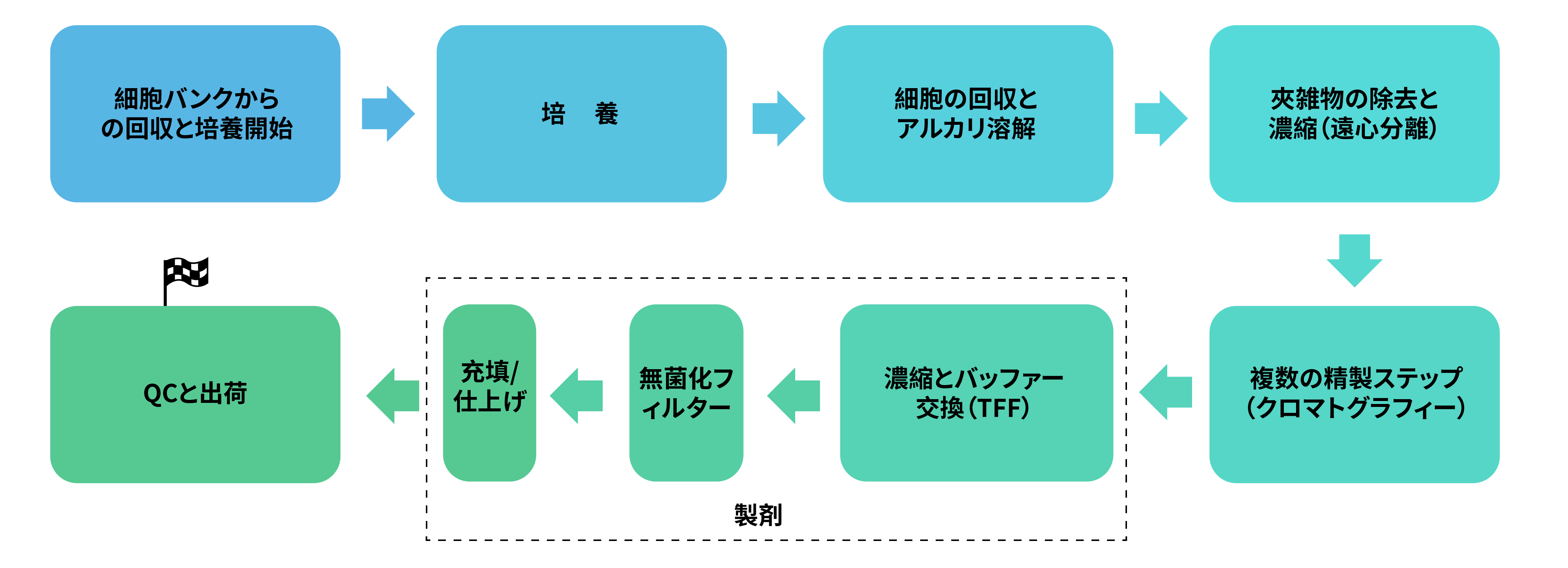
最大100Lの培養システムから、1バッチあたり最大5gの収量でプラスミドを製造することが可能です。一般的な製造工程を以下に示します:
品質検査アッセイ
以下のリストは、GMPプラスミドのリリースに関する主なQCアッセイをまとめています。同様のアッセイは、必要性に応じてGMP-likeプラスミドにもカスタムサービスとしてご提供しています。
品質/安定性検査開発サービスを読む-
一般/物理的特性
外観、濃度、pH、抽出量、浸透圧、凝集度
-
アイデンティティ
制限酵素処理、サンガーシークエンス
-
純度
- OD260/280
- スーパーコイルプラスミド比率: アガロースゲル電気泳動、キャピラリー電気泳動
- 残留タンパク質: BCA、SDS-PAGE
- ホスト大腸菌DNA: qPCR、アガロースゲル電気泳動
- ホスト大腸菌RNA: アガロースゲル電気泳動、 RT-qPCR、 蛍光定量
- 残留抗生物質: 比濁アッセイ、イムノアッセイ
-
セイフティー
- 滅菌性: 直接接種
- エンドトキシン: キネティッククロモジェニックアッセイ (KCA)
安定性検査
薬物安定性試験はICHガイドラインに従って実施します。強制分解研究はプラスミドDNAの品質属性に対する光、温度、pHなどの影響を評価します。



