IVT mRNAとLNP(脂質ナノ粒子)カプセル化

VectorBuilderは、医療目的のin vitro転写(IVT)mRNA製造および脂質ナノ粒子(LNP)開発を全工程でサポートするCROおよびCDMOサービスを提供しています。革新的な ベクターデザインプラットフォーム と豊富な経験をもとに、様々な研究・臨床ニーズに合わせた最適なin vitro転写ベクターデザイン、大規模なIVT mRNA製造、LNPカプセル化、徹底した品質管理をご提供しています。創薬研究、前臨床試験など、さまざまなダウンストリームニーズに対応した複数のグレードを用意しています。
IVT mRNA製造のワークフロー
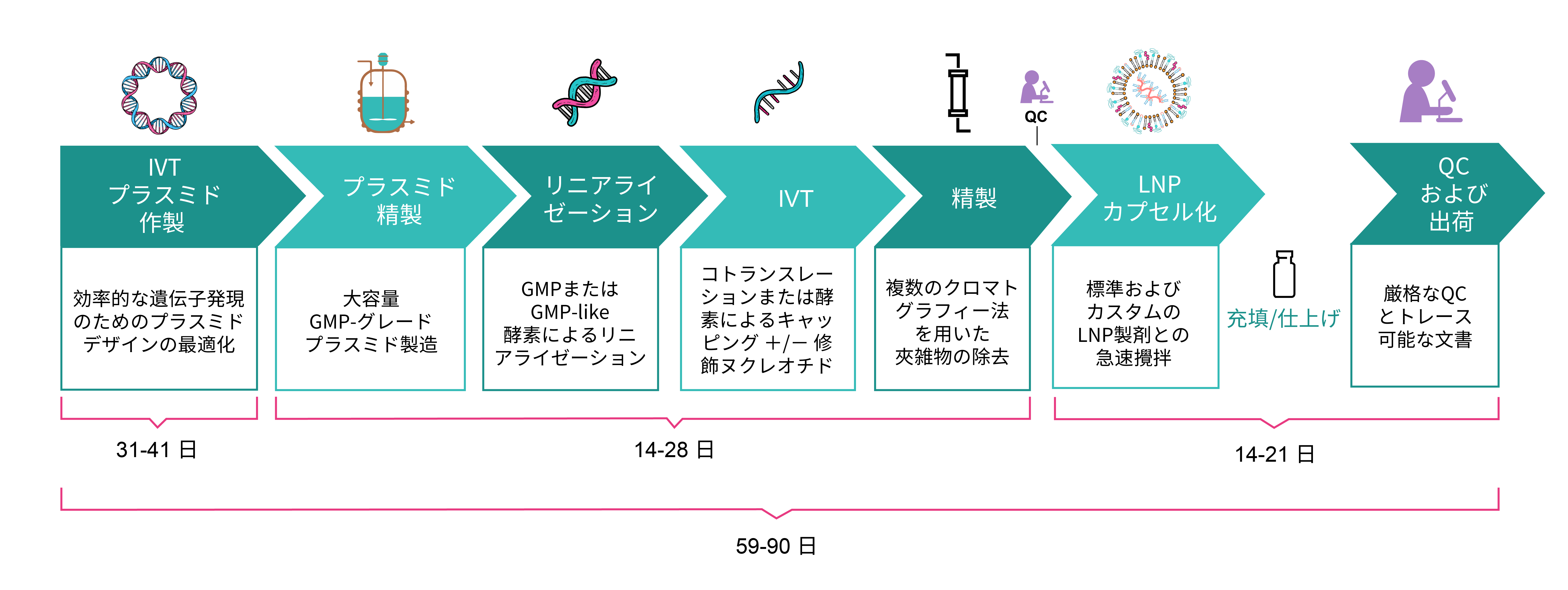
ご提供しているIVT mRNAのグレード
-
リサーチグレードmRNA
リサーチグレードのmRNAは、基礎研究および創薬研究用として開発されました。標準的な実験室の条件下で、厳格なQCにより製造されており、下流のあらゆる研究ニーズに適した高品質を保証しています。
リサーチグレードmRNAの詳細はこちら -
GMP-like mRNA
GMP-like mRNAは、医薬品の安全性や代謝に関する動物実験などの前臨床試験を対象としています。GMPガイドラインの主要な特徴に従って同等に製造されており、同様の製造工程と品質属性を有しています。製造は隔離された製造室で行われ、文書管理、トレーサビリティが確保されています。GMP-like グレードは、最終的なGMP製品の小規模な模倣品と見なすことができますが、はるかに低コストで、より迅速なタイムラインを実現します。必要に応じて、GMP-like mRNAは、RNaseフリーの培養および精製条件下で製造することができます。製品リリース時に品質検査証明書(COA)をご提供いたします。TSE/BSEステートメントは、ご要望に応じて発行いたします。
-
GMP-グレード mRNA Coming soon
GMPグレードのmRNAは、GMPガイドラインを厳守し、当社の認定GMPスイートで製造されています。製造工程では、包括的な品質保証システムが導入されています。幅広いインプロセスおよびリリースQCアッセイを実施し、mRNAが必要とされる品質および安全基準を満たすか、それ以上であることを確認します。製品リリース時には、製造工程を完全に記録したバッチリリースレポートとCOAをご提供しています。その他の文書については、ご要望に応じてご提供します。
IVT mRNAのグレード別比較
| リサーチグレード | GMP-like | |
|---|---|---|
| アプリケーション(用途) | 基礎研究, 治療薬開発, および 前臨床研究 | 薬物の安全性や代謝に関する動物を使った前臨床試験、GLP試験 |
| 製造スケール | mRNA: 0.1-10 mg LNP: 0.1-3 mg |
mRNA: 0.01-5 g LNP: 3-20 mg |
| 作業日数 | 49-71 日 ‧ ベクターデザインとクローニング: 26-36 日 ‧ プラスミド作製とリニアライゼーション: 14-21 日 ‧ IVT mRNA生産: 14-21 日 ‧ LNPカプセル化: 9-14 日 |
59-90 日 ‧ ベクターデザインとクローニング: 31-41 日 ‧ プラスミド作製とリニアライゼーション: 14-28 日 ‧ IVT mRNA生産: 14-28 日 ‧ LNPカプセル化: 14-21 日 |
| 品質管理システム | ISO9001 | GMP製造の主要な特長を取り入れた ISO9001 |
| 製造場所 | 標準的な実験室での並行生産 | 隔離された製造スイートで製造 |
| 文書管理とトレーサビリティ | なし | あり |
| QCおよび出荷時検査 | 標準QC | 個々のプロジェクトのニーズに合わせて実施 (下記参照) |
| 無菌充填 | N/A | 要望があれば可能 |
| サンプルの保存 | 要望があれば可能 | 要望があれば可能 |
| Other deliverable | COA | 1. COA 2. 製造サマリー 3. TSE/BSE文書(要望があった場合のみ) |
LNP(脂質ナノ粒子)カプセル化
VectorBuilderは、脂質ナノ粒子の混合と製造、および徹底した品質管理のための機器一式を完備した施設を有します。当社の製造スイートは、カスタム脂質製剤に対応し、マイクロ流体混合、希釈、バッファー交換、無菌ろ過、充填/仕上げを最先端の装置で行うことができます。
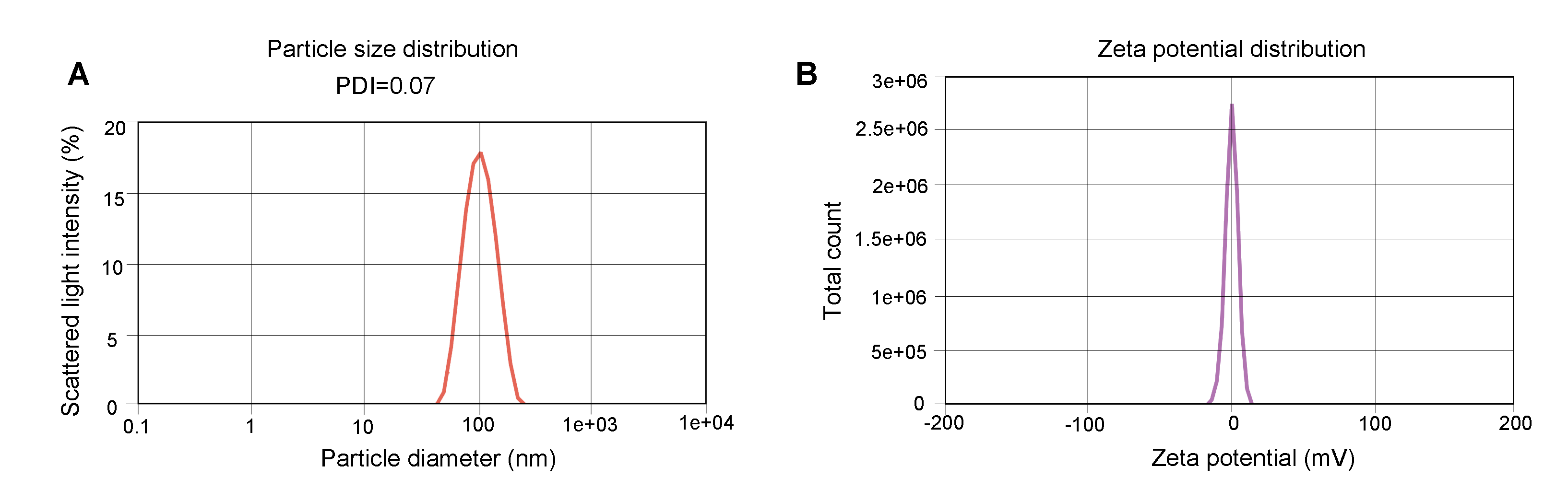
図1. 代表的なLNP-mRNA QC結果
(A) 粒子サイズは粒子の運動による光の散乱強度差を測定する動的光散乱(DLS)によって決定された。多分散インデックス(PDI)は、試料の粒子サイズの異質性を反映する。(B) ゼータ電位はLNPの安定性を反映し、-1.872 mVから+1.872 mV範囲で計測された。
品質検査アッセイ
| 製品 | 属性 | 分析方法 |
|---|---|---|
| IVT DNA テンプレート | 濃度 | 分光測定 |
| アイデンティティ(特性) | ゲル電気泳動、サンガーシークエンシング | |
| リニアライゼーション | キャピラリーゲル電気泳動 | |
| 宿主E. coli DNAの残留 | qPCR | |
| mRNA | 濃度 | UV-Vis分光測定 |
| インテグリティ(完全性) | キャピラリーゲル電気泳動、逆転写後にサンガーシークエンシング | |
| Capping効率 | LC-MS, キャピラリーゲル電気泳動 | |
| PolyA tailインテグリティ | LC-MS, キャピラリーゲル電気泳動 | |
| 残留タンパク質 | NanoOrange アッセイ | |
| 残留プラスミドDNA | qPCR | |
| dsRNA | ドットブロット | |
| エンドトキシン | キネティッククロモジェニックアッセイ (KCA) | |
| LNP | エンドトキシン | キネティッククロモジェニックアッセイ (KCA) |
| カプセル化効率 | RiboGreenアッセイ | |
| 直径, PDI(多分散度指数), およびゼータ電位 | Zetasizer |
ご提供している関連商品
VectorBuilder では、mRNA に加え、CRISPR 遺伝子編集用の IVT Cas9 mRNA および sgRNA、自己増幅 mRNA (saRNA) を提供しています。LNP製剤は、IVT mRNA分子、siRNA、プラスミドDNAのカプセル化に使用でき、複数の方法での遺伝子導入を可能にしています。



